세포의 성장과 증식 및 분화에 관여하는 단백질인 성장인자(growth factor). 종류에 따라 표적세포의 표면에 위치하는 특정 수용체(receptor)와 결합해 세포의 신호전달 물질로 작용하는 이 물질은 뼈세포 분화를 촉진하는 뼈형성단백질이나 혈관 분화를 촉진하는 섬유아세포증식인자, 혈관 내피 성장 인자 등이 대표적이다.
성장인자는 재생의학에 큰 발전을 가져왔다. 하지만 임상적으로 적용하기 위해서는 효능과 부작용 사이에서 상충되는 문제점이 많았기에 이는 늘 해결해야 할 과제로 인식되곤 했다.
성장인자의 효과적인 생체 내 전달
국내 연구진이 성장인자를 생체 내로 전달할 수 있는 새로운 작용기전의 원천기술을 개발해 주목을 받고 있다. 김희진, 육종인, 김남희 연세대 치과대학 교수팀이 연구를 진행한 결과 분해되기 쉬운 성장인자의 안정적인 전달을 도운 것이다. 이에 따라 조직재생이 필요한 악안면기형, 만성신장질환 같은 질환치료 연구에 새로운 단서를 제공할 것으로 기대를 받고 있다.
질병이 발생할 경우 일반적인 치료방법은 증상을 해소하거나 원인을 제거하는 데 집중한다. 하지만 성장인자를 이용한 치료방법은 기능이 저하되거나 손상된 세포, 혹은 조직 재생을 돕는 방식으로 진행한다. 이를 일컬어 '재생의학' 이라고 언급한다.
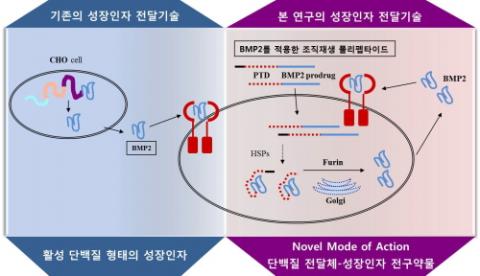
그러나 이미 학계에도 많이 알려진 BMP2(Bone morphogenetic protein 2, 뼈와 연골형성에 중요한 TGF-β계열의 성장인자), FGF 같은 성장인자들은 세포 내에서 쉽게 분해되므로 높은 농도의 투여가 필요했다. 그러다보니 실제 임상적용에 한계가 있던 것은 당연했다. 김희진 교수팀은 연구를 통해 세포막을 통과하는 단백질 전달체를 이용, 전구약물 형태의 성장인자를 융합시킨 후 세포 및 생체 내로 성장인자가 성공적으로 전달되는 것을 확인할 수 있었다.
"저희팀이 개발한 이번 연구기술은 전구약물(prodrug) 형태로 성장인자를 전달하는 새로운 작용기전을 갖는 성장인자 전달 원천기술입니다. 세포 내에서 전구약물 형태로 성장인자를 유도할 수 있는 단백유도체를 ‘조직재생 폴리펩타이드(Tissue Regenerative Polypeptides, TRP)’라고 이름을 붙였습니다. 일단 세포 내로 조직재생 폴리펩타이드가 전달되면 생체 내부에서 자연적으로 만들어지는 단백질의 일반적인 공정 과정과 똑같이 단백질 공정 과정을 거쳐 성숙한 단백질로 전환되게 됩니다. 이에 따라 생물학적인 성장인자 분비가 유도되게 되죠."
해당 연구로 개발된 '조직재생 폴리펩타이드'는 최근 여러 가지 약물 및 화장품 개발에 적용되고 있는 단백질 전달체(Protein transduction domain, PTD)를 포함하고 있다. 이에 따라 수용체와 결합에 의하지 않고 성장인자를 세포 내로 전달할 수 있다. 단백질 전달체 시스템을 이용한 만큼 전달하려는 성장인자의 크기 제한을 받지 않으며 면역성에 대한 문제도 없다.
"단백질 전달체는 10~16개의 염기성 아미노산으로 이뤄진 펩타이드로, 수용체와 결합하지 않고 세포막을 통과해 세포 내에 축적되는 물질입니다. 전달체와 전구약물 형태의 성장인자가 결합된 조직재생 폴리펩타이드는 성숙된 상태로 투여하는 기존의 성장인자와 달리 비활성 상태로 제작하기 때문에 경제적이고 임상에서 취급이 용이할 것으로 기대되고 있습니다."
성장인자 치료가 적용되는 경우는 매우 다양하다. 대표적인 것이 턱얼굴기형과 만성신부전 치료다. 김희진 교수는 "턱얼굴기형 환자에게는 국소적인 뼈재생이 필요할 수 있다. 이런 경우에 뼈형성인자를 이용한 조직재생 폴리펩타이드가 효과적인 뼈재생을 유도하는 데 이용될 수 있다"며 "만성신부전 환자는 질병이 진행됨에 따라 신장의 섬유화가 나타난다. BMP7을 이용한 조직재생 폴리펩타이드가 신장 섬유증을 되돌려 신장기능을 회복하는데 효과적으로 적용될 수 있을 것으로 판단된다"고 이야기 했다.
이처럼 질병 치료에 유익하게 사용될 수 있는 방법인 만큼, 이에 대한 연구는 활발하게 이뤄졌다. 그러나 한계가 작용해 어느 이상으로는 연구가 어려웠다. 그 한계는 바로 부작용이었다.
"성장인자는 대부분 수용성입니다. 때문에 성숙한 상태로 투여하게 되면 초기에 폭발적 방출이 일어나고 혈류에 의해 세척되며 효소작용에 의한 분해작용이 일어나 반감기가 짧아지게 됩니다. 따라서 원하는 효능을 얻기 위해 용량을 높여 적용하다 보면 여러 가지 부작용이 생길 수 있습니다. 효능과 부작용 사의의 상충되는 문제점을 해결하기 위해 성장인자의 운반체(carrier) 개발에 대해 연구들이 집중되고 있지만 성장인자 자체가 수용성을 띠기 때문에 근본적인 문제점은 여전히 남아 있는 상태였죠."
이를 해결하기 위해 김희진 교수팀은 새로운 아이디어를 제시했다. 수용성을 띠는 성숙한 성장인자가 가진 생체 적용의 한계점을 극복하기 위해서는 비수용성 물질을 사용하면 되겠다고 생각, 그렇다면 성숙한 약물 형태가 아닌 전구약물(prodrug) 형태의 성장인자를 만들고 세포 내로 전달된 후에 성숙한 형태로 바뀌도록 하면 되지 않을까 생각한 것이다.
다소 엉뚱한 발상처럼 보이지만 김희진 교수팀은 연구에 연구를 거듭해 결국 이에 성공할 수 있었다. 세포 실험에서 조직재생 폴리펩타이드의 새로운 작용기전을 확인했으며, 생체 실험에서도 뛰어난 효능을 보인다는 사실을 검증했다.
골재생 유도 사실 확인
그렇다면 개발한 기술의 성능은 어느 정도라고 할 수 있을까. 김희진 교수는 "조직재생 폴리펩타이드 제작 기술에 BMP2를 적용해 생체 효능 실험을 시행했을 때 마이크로그램(ug) 단위로도 골재생이 유도되는 것을 확인할 수 있었다"며 "이는 기존의 재조합 BMP2 농도의 1/1000 이하에서도 골재생이 유도된 것을 검증한 결과"라고 이야기 했다.
"뿐만 아니라 같은 방법으로 세포의 이동성을 조절하는 것으로 알려진 다른 성장인자(BMP7, DKK1)도 효과적으로 생체 내로 전달돼 암세포의 이동과 침윤을 억제하는 것을 확인했습니다. 그동안 성숙된 단백질의 형태가 아닌 전구약물 형태의 성장인자를 전달하고자 시도했던 전례는 없었습니다. 저희팀의 연구는 전구약물 형태로 성장인자를 세포 내로 전달했기 때문에 성공했다고 말할 수 있어요. 생체 내에서 자연적으로 만들어지는 단백질과 똑같이 일반적인 단백질 공정 과정을 거치게 되고 생물학적인 성장인자 분비가 유도되기 때문이죠."
김희진 교수팀이 이번 연구를 진행한 것은 기존의 연구가 해결하지 못하는 기술의 한계를 극복하기 위해서였다. 그간 구강악안면 영역에서 뼈재생을 유도하려는 시도는 오래 전부터 있었지만, 다양한 뼈 이식재 중 생물학적인 골유도는 오직 자가골 이식과 BMP2에서만 보고되고 있다.
"1988년 HIV-1 TAT을 이용한 PTD 기반의 단백질 유도체 기술이 처음으로 보고되면서 수용체와 결합하지 않고 세포막을 통과해 세포 내로 단백질을 전달할 수 있는 방법에 대한 연구가 활발했습니다. PTD를 이용해 BMP2를 세포 내로 전달할 생각을 했죠. 세포 내에서 이뤄지는 자연적인 단백질 공정 과정을 그대로 모방하기 위해 BMP2를 성숙한 형태가 아닌 전구약물 형태로 만들려고 했던 발상의 전환이 중요했다고 생각합니다."
총 10년이 걸린 연구다. 육종인 교수 팀에서 BMP2 조직재생 폴리펩타이드를 제작하고 세포 내 초기 효능을 확인하는 데 3년이 걸렸고, 이후 생체 내 효능 확인 실험에 7년이 걸렸다.
"정말 오랜 시간이 걸렸습니다. 시간이 오랜 만큼, 어려움도 많았어요. 연구비 지원이 없어 비용이 많이 드는 동물실험을 계속 진행하는 것도 어려웠지만, 그보다 더 힘들었던 것은 확신을 유지하는 일이었습니다. 생체 효능 결과를 내기가 무척 어려웠어요. 헌데 실험결과가 실패로 나오자 같이 연구를 진행한 한 연구자는 저희를 사기꾼으로 취급하기도 했죠. 지금 돌이켜 보면 당시는 조직재생 폴리펩타이드 자체의 순도도 부족하고 동물실험 디자인도 많이 부족했기 때문인 것 같아요. 하지만 그럼에도 불구하고 단단한 과학적 증거가 있었기에 확신을 가질 수 있었고 실패가 있어도 포기하지 않을 수 있었습니다."
김희진 교수는 "기존의 수용성 성장인자의 한계를 극복한 것은 물론 새로운 작용기전의 성장인자 전달을 이용한 신의료기술 개발이 가능할 것으로 본다"며 "본 연구에서 예를 든 세 가지 성장인자의 임상적용 가능성을 생각해 보자면, BMP2 조직재생 폴리펩타이드는 구강악안면 영역뿐 아니라 신경외과, 정형외과 영역에서 뼈재생에 활용될 수 있을 것으로 판단된다. BMP7은 조직재생 폴리펩타이드는 신장섬유증과 같은 만성신장질환에서 사용될 수 있을 것으로 예상된다. 마지막으로 DKK1은 주요 암발생 신호전달을 억제하는 역할을 하는 물질이므로 DKK1 조직재생 폴리펩타이드는 항암치료기술에서 사용될 수 있을 것으로 예상된다"고 언급했다.
새로운 작용기전의 성장인자 전달 원천기술로써, 차세대 성장인자를 전달하는 신의료기술 개발의 가능성을 제시한 연구. 김희진 교수는 앞으로 좀 더 낮은 농도에서도 생체 효능이 가능한 지 확인해 보고 싶다고 이야기 했다. "임상적으로 적용이 쉽도록 주사기 형태로 제조해 효능 확인을 해보고 싶습니다. 또 많은 비용이 들겠지만 다른 성장인자(BMP2)에 대해서도 중형동물 실험을 시행해 보고 싶다"고 바람을 덧붙였다.
- 황정은 객원기자
- hjuun@naver.com
- 저작권자 2014-10-28 ⓒ ScienceTimes
관련기사

 뉴스레터
뉴스레터